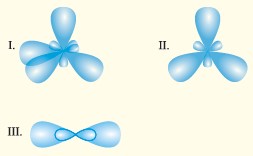
В молекуле алкена после образования
σ-связи между атомами углерода р орбитали этих атомов притягивают друг друга. За счёт образования π-связи при перекрывании этих орбиталей ядра атомов углерода приближаются друг к другу ещё ближе.
σ-связи между атомами углерода р орбитали этих атомов притягивают друг друга. За счёт образования π-связи при перекрывании этих орбиталей ядра атомов углерода приближаются друг к другу ещё ближе.

В результате расстояние между ядрами углерода уменьшается. В молекуле этана
длина связи С - С равна 0,154 нм, а в молекуле этена длина связи С = С составляет
0,134 нм. И ещё при образовании π-связи площадь перекрывания орбиталей бывает
меньше, чем в σ-связи.
Поэтому энергия и прочность π-связи меньше, чем в σ-связи. А энергия двойной
связи меньше энергии двух σ-связей.


Проверьте изученное
-
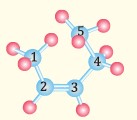
Определите по шаростержневой модели молекулы атомы углерода, находящиеся в sp2 гибридном состоянии.
-
Определите, в какой последовательности увеличивается число гибридных орбиталей в данном ряду веществ.1. метан 2. этан 3. этенA) 1, 2, 3
D) 2, 3,1B) 1, 3, 2
E) 3, 2,1C) 2,1, 3
-
Как можно объяснить отличия пространственного строения молекул этана и этена?
-
Какими электронными облаками обладают атомы углерода молекулы пропена? Обоснуйте свои мысли.