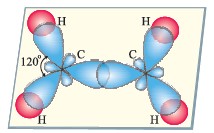
Две гибридные орбитали каждого атома углерода, перекрываясь с s-орбиталями атомов водорода (sр2 - s перекрывание), образуют С - Н связи. Третьи гибридные орбитали атомов углерода, перекрываясь вдоль прямой линии, соединяющей центры ядер атомов, образуют С - С σ-связь (sр2 - sр2 перекрывание).
Как видно, в отличие от молекул этана, атомы
углерода в молекулах этена расположены на
одной плоскости. В атомах углерода, не принявших
участия в гибридизации, р-орбитали
направлены перпендикулярно к плоскости,
в которой находятся орбитали, образующие
сигма связи. Эти орбитали за счёт бокового
перекрывания между собой выше и ниже плоскости,
в которой находятся атомы, образуют
вторую - π (пи) связь (р-р перекрывание).
Ниже даны шаростержневая и шаровая модели молекулы этена.

Шаростержневая
модель молекулы этена
модель молекулы этена
Шаровая модель
молекулы этена
молекулы этена


Обсуждение