Деятельность
1
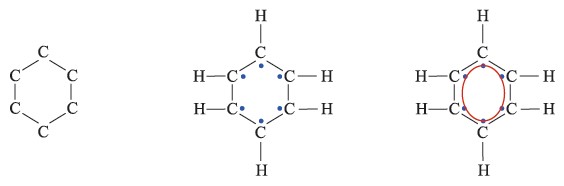
На основе формулы, предложенной Кекуле, длина одинарной связи должна соответствовать
0,154 нм (как в алканах), а длина двойной связи - 0,134 нм (как в
алкенах).

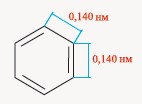
Тем не менее, исследования показали, что все связи между атомами углерода
в молекуле бензола короче одинарной связи (0,154 нм), длиннее двойной связи
(0,134 нм) и составляют 0,140 нм.

Как можно объяснить причину этого?
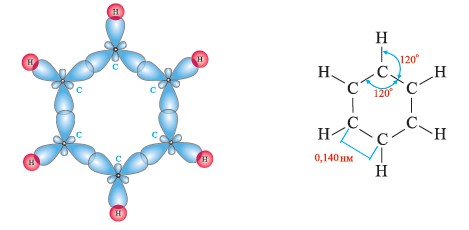
Согласно современным представлениям все атомы углерода в молекуле бензола находятся в sp2 гибридном состоянии.
За счёт двух гибридных
орбиталей каждый
углеродный атом образует
σ-связь с двумя соседними
углеродными атомами, и
образуется циклическое
строение.
орбиталей каждый
углеродный атом образует
σ-связь с двумя соседними
углеродными атомами, и
образуется циклическое
строение.
За счёт другой гибридной
орбитали каждый углеродный
атом образует σ-связь с одним
водородным атомом. У каждого
углеродного атома имеется одна
негибридная орбиталь.
орбитали каждый углеродный
атом образует σ-связь с одним
водородным атомом. У каждого
углеродного атома имеется одна
негибридная орбиталь.
За счёт негибридных р
орбиталей углеродных
атомов образуется одна
шестиэлектронная π-система
орбиталей углеродных
атомов образуется одна
шестиэлектронная π-система
Орбитали углеродных атомов, образующие связь, находятся на одной плоскости
и соединяются друг с другом под углом 120°. Поэтому σ-связи в молекуле бензола
образуются на одной плоскости. Так как все углеродные атомы образуют одинаковые
гибридные орбитали, то они имеют и одинаковую длину связи (0,140 нм).
А бензольное кольцо имеет форму правильного шестиугольника.