
Metan molekulu əmələ
gələn zaman bütün rabitə
bucaqları 109°28' olur.
gələn zaman bütün rabitə
bucaqları 109°28' olur.
Tsiklopropan molekulu əmələ gələn zaman karbon atomları
arasında hibrid orbitalların qapanması nəticəsində rabitə
bucağı kiçilir və 60° olur.
arasında hibrid orbitalların qapanması nəticəsində rabitə
bucağı kiçilir və 60° olur.
Tsikloalkan molekullarında karbon atomları arasında rabitə yaradan hibrid orbitallar alkanlar
ilə müqayisədə gərilmiş vəziyyətdə olur (bu rabitələrə bəzən “banan” rabitəsi də
deyilir). Bu gərilmə karbon atomları arasında olan valent bucağının normal vəziyyətdən
('lOƏ^Sə kənaraçıxmasının artması ilə artır. Bu kənaraçıxma bucaq gərginliyi adlanır.
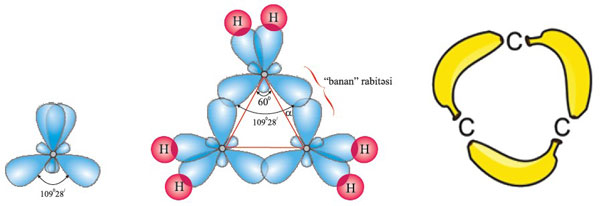
Hibrid orbitalların gərilməsi hesabına
valent bucağı 109°28,-dən 60°-dək azalır.
valent bucağı 109°28,-dən 60°-dək azalır.
Tsiklopropan molekulunda
“banan” rabitəsi
“banan” rabitəsi
Digərtsikloalkan molekullarının əmələ gəlməsi zamanı da rabitə bucağı 109°28-dən fərqli
olur. Məsələn, tsiklobutan molekulunda rabitə bucağı 90°, tsiklopentan molekulunda
108°, tsikloheksan molekulunda isə 120° olur. Aşağıda tsiklopropan və tsiklobutan molekullarının
mil-kürəcik modelləri verilmişdir.

tsiklopropan molekulunun
mil-kürəcik modeli
mil-kürəcik modeli
tsiklobutan molekulunun
mil-kürəcik modeli
mil-kürəcik modeli
Tsikloalkanlarda tsiklin ölçüsü böyüdükcə bucaq gərginliyi azalır.