Odur ki ideal qaz istənilən qədər sıxıla bilir;
− Molekulları arasındakı qarşılıqlı cazibə xarakterli qüvvələr nəzərə alınmayacaq dərəcədə zəifdir;
− Molekulları arasında itələmə xarakterli qüvvələrdir, onlar yalnız bir-biri ilə toqquşduqda meydana çıxır; molekulların toqquşmaları mütləq elastiki qəbul edilir;
− Molekulları ixtiyari sürət ala bilər, hər bir molekulun hərəkəti klassik mexanika qanunlarına tabedir.
İdeal qazın xassələri mikroskopik və makroskopik parametrlər və onlar arasındakı
əlaqələrlə xarakterizə olunur.
● Qazın əsas mikroskopik parametrləri - qaz molekulları və onların hərəkətini xarakterizə edən
parametrlərdir. Bu parametrlərə molekulun kütləsi, onun sürəti, impulsu və irəliləmə hərəkətinin
kinetik enerjisi aiddir.
● Qazın makroskopik parametrləri - qazın bütövlükdə xassələrini müəyyən edən təzyiq, həcm və
temperaturdur.
Molekulyar-kinetik nəzəriyyənin əsas məsələsi qazın makroskopik və mikroskopik parametrləri arasında əlaqə yaratmaqdır.
İdeal qazın molekulyar-kinetik nəzəriyyəsinin əsas tənliyi. Bilirsiniz ki, qapalı qabda yerləşən qazın molekullarının qabın divarına fasiləsiz olaraq vurduqları çoxsaylı nizamsız zərbələr nəticəsində qazın təzyiqi yaranır. Bu təzyiq vahid səthə təsir edən əvəzləyici qüvvənin modulunun orta qiymətinə bərabərdir:
p = F
S .
Alman fiziki Rudolf Klauzius (1822-1888) ideal qaz modelindən istifadə etməklə 1857-ci ildə qazın
təzyiqini - ideal qazın molekulyar-kinetik nəzəriyyəsinin əsas tənliyini müəyyənləşdirir.
● İdeal qazın molekulyar-kinetik nəzəriyyəsinin əsas tənliyi - qazı xarakterizə edən makroskopik
parametr olan təzyiqi onun molekullarını xarakterizə edən mikroskopik parametrlərlə əlaqələndirən
tənlikdir:
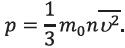 (6.1)
(6.1)
Molekulun xaotik hərəkətində hər üç istiqamətin “eyni ehtimallı”dır. Burada m0
— bir
molekulun
kütləsi, n -
molekullarının konsentrasiyası, ʋ2 - molekulların sürətinin
kvadratının orta qiymətidir.
● Molekulların konsentrasiyası - vahid həcmdə olan molekulların sayıdır:
n = N
V . (6.2)
Konsentrasiyanın BS-də vahidi: [n] = 1
m3
=
m-3.
● Molekulların orta kvadratik sürəti (vor.kv) - molekulların sürətinin kvadratının
orta qiymətinin kvadrat köküdür:
