Fiziki xassələri. Ammonyak – rəngsiz, xarakterik kəskin iyli, havadan təqribən 2 dəfə yüngül qazdır. Yüksək təzyiqdə və ya soyudulduqda o, asanlıqla rəngsiz mayeyə çevrilir (tqay. = –33,4°C). Maye ammonyak böyük buxarlanma istiliyinə malikdir və bu səbəbdən soyuducu qurğularda tətbiq edilir. Ammonyak suda yaxşı həll olur (20°C-də 1l suda 700 l ammonyak həll olur). Ammonyakın suda 10%-li məhlulu ammonyaklı su və ya naşatır spirti adlanır.
Kimyəvi xassələri. Ammonyakın suda məhlulu zəif qələvi xassəlidir, çünki ammonyak molekullarının az bir hissəsi su ilə reaksiyaya girib məhlulda NH4+ və OH– ionları əmələ gətirir (e):
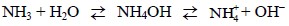
əmələ gətirir (f):

Qatı xlorid turşusuna salınmış şüşə çubuğu ammonyakla dolu sınaq şüşəsinin ağzına yaxınlaşdırdıqda ammonium- xlorid duzunun hissəciklərindən ibarət ağ tüstü əmələ gəlir (f):

Yuxarıda baxılan reaksiyalarda azotun oksidləşmə dərəcəsi dəyişmir, valentliyi isə III-dən artıb IV olur.
Ammonyakın digər reaksiyalarında azotun oksidləşmə dərəcəsi dəyişir.
Ammonyak qızdırıldıqda parçalanır:
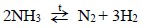
Ammonyak saf oksigendə sarı alovla yanır, havada isə yanmır. Qızdırılmış hava və katalizatorun iştirakında ammonyak azot-monooksidə oksidləşir:

İkinci reaksiyadan nitrat turşusu istehsalında istifadə edilir.
Ammonyak karbon-dioksidlə azot gübrəsi – karbamid CO(NH2)2 əmələ gətirir:


