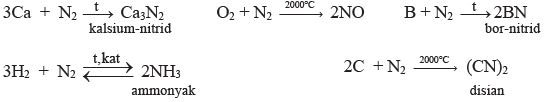Kimyəvi xassələri. Azot (N2) adi şəraitdə az fəaldır; buna görə azot təbiətdə sərbəst halda yayılmışdır. Azotun az fəal olması onun molekulunda N≡N rabitəsinin kifayət qədər davamlılığı ilə bağlıdır. Bu səbəbdən azot (N2) yalnız yüksək temperaturda metal və qeyri-metallarla reaksiyaya girir. Litium azotla adi şəraitdə reaksiyaya daxil olur:
Azot bir neçə oksid əmələ gətirir. Bu oksidlərdə azotun oksidləşmə dərəcəsi +1-dən +5-dək dəyişir:

Oksidlərdən N2O və NO duzəmələgətirməyən, qalanları isə turşu oksidləridir. Bu oksidlərdən yalnız azot-monooksid NO azotun oksigenlə bilavasitə qarşılıqlı təsirindən alınır. O, yüksək temperaturda və ya atmosferdə ildırım çaxarkən yaranan elektrik boşalması zamanı əmələ gəlir.
Diazot-trioksidə N2O3 – nitrit turşusu HNO2, diazot-pentaoksidə N2O5 – nitrat turşusu HNO3 uyğun gəlir. Azot-dioksid NO2 su ilə iki turşu – nitrat HNO3 və nitrit HNO2 turşularını əmələ gətirir:
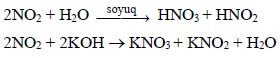
Bu səbəbdən azot-dioksid NO2 qarışıq anhidrid də adlanır.
Azot-dioksidi artıq miqdarda götürülmüş oksigenin iştirakı ilə suda həll etdikdə yalnız nitrat turşusu alınır (bax: səh. 99):
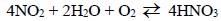
Azot-dioksid NO2 – qonur rəngli, spesifik iyli, havadan ağır, zəhərli qazdır.
Tətbiqi. Azot, əsasən, ammonyakın alınmasına, ondan isə nitrat turşusu, mineral gübrələr, partlayıcı maddələr və s. istehsalına sərf olunur.
Azotdan təsirsiz mühit yaradılmasında - elektrik lampalarında, havaya və rütubətə həssas olan maddələrin saxlanmasında və daşınmasında geniş istifadə olunur. Azotla həmçinin polad əşyaların səthi yüksək temperaturda azotlaşdırılır.