Allotrop şəkildəyişmələri. Kükürdün 2 allotrop şəkildəyişməsi mövcuddur: kristallik və plastik (amorf) kükürd. Adi şəraitdə kristallik kükürd daha davamlıdır; ona görə də zaman keçdikcə plastik kükürd tədricən kristallik kükürdə çevrilir.
almaq üçün qaynama temperaturuna
qədər qızdırılmış kükürdü soyuq
suya tökürlər. Bu zaman rezin kimi
dartıla bilən kükürd əmələ gəlir.
Fiziki xassələri. Kristallik kükürd sarı rəngli, kövrək, sudan iki dəfə ağır, 112,8°C-də əriyən və 444,6°C-də qaynayan bərk maddədir. Qeyri-metal kimi o, istiliyi pis keçirir, elektrik cərəyanını isə keçirmir. Kükürd suda həll olmur, lakin karbon-disulfiddə CS2 yaxşı həll olur.
Toz halında olduqda kükürd suda islanmır və bu səbəbdən suyun üzərində üzür. Xırdalanmış halda bu xassəyə həmçinin kükürdün bir çox təbii birləşmələri də malikdir. Ona görə də suda islanıb çökən “boş süxur”lardan kükürd filizlərinin ayrılmasında bu xassədən sənayedə istifadə edilir. Filizlərin bu cür zənginləşdirilməsi üsuluna flotasiya deyilir.
Kimyəvi xassələri. Kükürd tipik qeyri-metaldır. Reaksiyalarda həm oksidləşdirici, həm də reduksiyaedici xassələr göstərir. (Kimyəvi tənliklərdə kükürd şərti olaraq S kimi göstərilir).
Kükürd – oksidləşdirici kimi. Kükürd qızıl, iridium və platindən başqa digər metalları və elektromənfiliyi kükürdün elektromənfiliyindən az olan qeyri-metalları oksidləşdirir. O, qələvi və qələvi-torpaq metalları, həmçinin civə ilə adi şəraitdə, digər metal və qeyri-metallarla isə əsasən qızdırıldıqda reaksiyaya daxil olur:
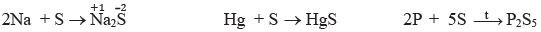
Kükürd – reduksiyaedici kimi. Kükürd oksigen və halogenlərlə birləşmələrində reduksiyaedici xassə göstərir. O, yod və azotla, həmçinin su ilə reaksiyaya daxil olmur: