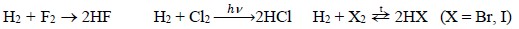Alınması. 1. Flüoru kalium-flüorid və ya kalsium-flüorid ərintisinin elektrolizindən almaq olar:

2. Xlorun alınması ilə səh. 63-də tanış oldunuz.
3. Brom laboratoriyada bromid turşusu və ya onun duzlarına oksidləşdiricilərlə (MnO2, KMnO4, KClO3 və s.) təsir etməklə alınır:
Sənayedə brom bromidlərə xlorla təsir etməklə alınır:
4. Yod laboratoriyada yodid turşusu və onun duzlarına zəif oksidləşdiricilərlə (Fe3+, Cu2+ və s.) təsir etməklə alınır:
Sənayedə yod yodidlərə xlorla təsir etməklə alınır:
Fiziki xassələri. Flüor və xlor müvafiq olaraq açıq-sarı və sarımtıl-yaşıl rəngli, zəhərli qazlardır. Brom – buxarı zəhərli olan qırmızı-qonur rəngli maye, yod – kəskin iyli, tünd-bənövşəyi rəngli, qızdırıldıqda asanlıqla sublimasiya edən bərk maddədir.
F2→Cl2→Br2→I2 sırasında atom və molekulların ölçüləri böyüdüyü üçün molekullararası cazibə qüvvələri artır. Bunun nəticəsi kimi bu sırada halogenlərin rəngləri tündləşir, sıxlıqları, ərimə və qaynama temperaturları artır.
Halogenlər suda az, spirtdə, benzində və ağ neftdə yaxşı həll olur. Flüor adi şəraitdə su ilə (dönməyən şəkildə) qarşılıqlı təsirdə olduğundan onun suda məhlulunu almaq mümkün deyil.
Kimyəvi xassələri. Halogenlərin kimyəvi aktivliyi flüordan yoda doğru azalır. Ona görə flüor başqa halogenlərə nisbətən daha şiddətli reaksiyaya daxil olur; məsələn, flüor adi şəraitdə karbon, fosfor, kükürd və bir çox metallarla şiddətli reaksiyaya girir:
Flüordan başqa, digər halogenlər, əsasən, qızdırıldıqda reaksiyalara daxil olur.
Hidrogen flüorla qaranlıqda partlayışla, xlorla işıq şüasının təsiri ilə və ya qızdırıldıqda, brom və yodla isə qızdırıldıqda (dönər reaksiya üzrə) qarşılıqlı təsirdə olur: