Təbiətdə yayılması. Xlor aktiv element kimi təbiətdə birləşmələr şəklində rast gəlinir. Onun əsas təbii birləşmələrinə qalit NaCl, silvin KCl, silvinit NaCl·KCl, karnalit KCl·MgCl2·6H2O və s. aiddir. Xlorun birləşmələrinə okean, dəniz və göl sularında, həmçinin bitki və heyvan orqanizmlərində də rast gəlinir.
Alınması. Laboratoriyada xloru xlorid turşusuna MnO2, KMnO4, K2Cr2O7 və KClO3 kimi qüvvətli oksidləşdiricilərlə təsir etməklə alırlar:
KClО3 + 6HCl → 3Cl2↑ + KCl +3H2O
Sənayedə xlor natrium-xloridin ərintisinin və ya suda qatı məhlulunun elektrolizindən alınır:

Fiziki xassələri. Xlor – sarımtıl-yaşıl rəngli, kəskin iyli boğucu zəhərli qazdır. Havadan 2,5 dəfə ağırdır. 20°C-də 1 l suda 2,5 l xlor həll olur. Xlorun suda məhlulu xlorlu su adlanır. Xlor tənəffüs yollarını qıcıqlandırır; onun uzun müddətdə böyük miqdarı ilə tənəffüs ölümlə nəticələnir. Xlor təzyiq altında mayeləşir və maye xlor polad balonlarda saxlanılır.
Kimyəvi xassələri. Xlor qüvvətli oksidləşdiricidir. O, oksigen, azot və karbon ilə bilavasitə qarşılıqlı təsirdə olmur. Xlor hidrogenlə işıqda (h𝜈), stibium (Sb) və fəal metallarla otaq temperaturunda, digər bəsit maddələrlə isə qızdırıldıqda qarşılıqlı təsirdə olub özünü oksidləşdirici kimi aparır:

| – | Hansı reaksiyalarda xlor oksidləşdiricidir? Xlorun bu reaksiyalarda oksidləşdirici xassə göstərməsinə səbəb nədir? |
| – | Hansı halda bəsit maddələrdən PCl3, hansı halda PCl5 birləşməsi alınar? |
| – | Sizcə, nə üçün dəmir xlorid turşusu ilə FeCl2, xlorla isə FeCl3 əmələ gətirir? |
| – | Hansı reaksiyaların məhsullarında xlorla birləşməsində element ikivalentlik göstərir? |
| Nə üçün bu birləşmələrin formulları bir-birindən fərqlidir? |
Xlorun mürəkkəb maddələrlə qarşılıqlı təsiri. Xlor su ilə reaksiyaya girərək xlorid və hipoxlorit turşularını əmələ gətirir:
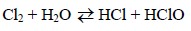
Alınan məhlul xlorlu su adlanır. Hipoxlorit turşusu davamsız olduğundan parçalanır. Onun parçalanmasından alınan atomar oksigen güclü oksidləşdirici olduğundan üzvi boyaları rəngsizləşdirir: