Oksigendə yandırıldıqda litium metalı – oksid (Li2O), natrium metalı – peroksid (Na2O2), kalium, rubidium və sezium isə MO2 tərkibli superoksidlər əmələ gətirir:
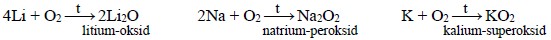
Qələvi metallar halogenlər və kükürdlə duzlar, hidrogenlə hidridlər əmələ gətirir:
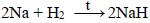
Litium azotla otaq temperaturunda, qalanları isə qızdırıldıqda nitridlər əmələ gətirir:
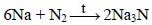
Qələvi metalların və onların hidridlərinin su ilə qarşılıqlı təsirindən hidrogen ayrılır:
Qələvi metallar aktivliyi az olan metalları onların duzlarının suda məhlulundan sıxışdırıb çıxarmır, çünki ilk növbədə qələvi metal su ilə reaksiyaya daxil olub qələvi əmələ gətirir.
Tətbiqi. Qələvi metallardan natrium əlvan metallurgiyada reduksiyaedici, nüvə
reaktorlarında isə istilikdaşıyıcı kimi tətbiq edilir. Ondan həmçinin kauçukun alınmasında
katalizator kimi istifadə olunur. Sezium işıq enerjisini elektrik enerjisinə
çevirən fotoelementlərdə tətbiq edilir.
Qələvi metallardan ən çox əhəmiyyət kəsb edəni natrium və kaliumdur.
Natrium, kalium və onların birləşmələri
Təbiətdə yayılması. Natriumun ən mühüm minerallarından qaliti NaCl, silviniti NaCl·KCl, Çili şorasını NaNO3, krioliti Na3[AlF6] və s.-ni göstərmək olar.
Kaliumun silvin KCl, silvinit NaCl·KCl və kainit KCl·MgSO4·3H2O kimi mineralları geniş yayılmışdır.
Alınması. Sənayedə natrium və kalium onların xloridlərinin (NaCl, KCl), ərintisinin elektrolizindən alınır:
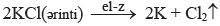
Fiziki və kimyəvi xassələri (bax: qələvi metalların fiziki və kimyəvi xassələri).
Na2O və K2O – əsasi xassəli bərk maddələrdir; onlar adi şəraitdə havanın su buxarı və karbon qazı ilə reaksiyaya daxil olur; su ilə qarşılıqlı təsirdə olduqda qələvilər əmələ gətirir:

NaOH və KOH çox hiqroskopik maddələrdir. Ona görə natrium və kaliumun həm oksidləri, həm də hidroksidləri ağzı kip bağlanmış qablarda saxlanılır.
