2KOH + CuSO4 + (H2) → Cu(OH)2↓ + K2SO4 + (H2↑)
Metalların kimyəvi xassələri
Metalların kimyəvi xassələri onların atomlarının öz valent elektronlarını asanlıqla verib, müsbət yüklü ionlara çevrilməsi qabiliyyəti ilə müəyyən olunur: M – ne- → Mn+ . Ona görə də kimyəvi reaksiyalarda metal atomları (M) həmişə reduksiyaedici xassə göstərir.
Gümüş, qızıl və platindən başqa, digər metallar oksigenlə qarşılıqlı təsirdə olur; bu zaman, adətən, oksidlər əmələ gəlir:
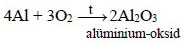

Azotla litium otaq temperaturunda, digər metallar isə qızdırıldıqda reaksiyaya daxil olub nitridlər əmələ gətirir:
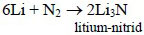
Qızdırıldıqda I və II qrupun əsas yarımqrup metalları (berilliumdan Be başqa) hidrogenlə hidridlər əmələ gətirir:
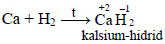
Metalların elektrokimyəvi gərginlik sırasında hidrogendən solda yerləşən metallar sudan hidrogeni sıxışdırıb çıxarır:
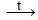 Fe3O4 + 4H2↑
Fe3O4 + 4H2↑
Qələvi və qələvi-torpaq metalları, həmçinin oksid təbəqəsi təmizlənmiş alüminium, məsələn, alüminium amalqaması su ilə qızdırılmadan qarşılıqlı təsirdə olur.