Kimyəvi xassələri. Metan kimyəvi cəhətdən az fəal maddədir. O, adi şəraitdə turşulara, qələvilərə, oksidləşdiricilərə qarşı davamlıdır, bromlu suyu və kalium-permanqanat məhlulunu rəngsizləşdirmir.
Metan əvəzetmə, oksidləşmə və parçalanma reaksiyalarına daxil olur.
I. Əvəzetmə reaksiyalarında C–H rabitəsi qırılır və H atomu digər atomla əvəz olunur. Məsələn, işığın (h𝜈) və ya temperaturun təsiri ilə xlor metan molekulundakı hidrogen atomlarını tədricən əvəz edərək müxtəlif xlorlu törəmələrin qarışığını əmələ gətirir:

Brom da metanla bu cür qarşılıqlı təsirdə olur.
II. Metan böyük miqdarda istilik ayırmaqla, demək olar ki, rəngsiz alovla yanır. Bu zaman karbon qazı və su əmələ gəlir:
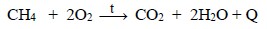
Metan hava ilə partlayış törədə bilən qarışıqlar əmələ gətirir. Belə qarışıqlar şaxtalarda və zavod qazanxanalarında, yaşayış mənzillərində yarana bilər.
Metanın su buxarı ilə konversiyasından sintez-qaz alınır:

III. Yüksək temperaturda metan parçalanır. Şəraitdən asılı olaraq ondan duda (his), asetilen (C2H2) və etilen (C2H4) qazları alınır:

Üzvi birləşmələrin molekullarından hidrogen molekulunun ayrılması reaksiyaları dehidrogenləşmə reaksiyaları adlanır.
Tətbiqi. Metan yanacaq kimi geniş tətbiq olunur. Ondan həmçinin hidrogen, duda, asetilen, sintez-qaz və s. alınır. Metandan metil spirti, sirkə turşusu, sintetik kauçuklar və sintetik benzinin alınmasında xammal kimi istifadə edilir. Metanın halogenli törəmələri soyuducu qurğularda, həlledici kimi, təbabətdə, yanğın söndürülməsində istifadə olunur. Maye propan və butandan nəqliyyatda, bəzən məişətdə də yanacaq kimi istifadə edilir.
Etilmerkaptan həmçinin propan və butan qazlarına da əlavə edilir.