Karbonun oksidləşmə dərəcəsi qeyri-üzvi birləşmələrində, əsasən, +4 (CO-da +2), üzvi birləşmələrində isə –4-dən +4-dək (sıfırda daxil olmaqla) dəyişir.
Təbiətdə yayılması. Təbiətdə karbona həm sərbəst (əsasən, almaz, qrafit), həm də birləşmələr şəklində rast gəlinir. Karbon havada olan karbon-dioksidin, həmçinin karbonatların – əhəngdaşının, təbaşirin, mərmərin (əsas tərkib hissəsi – CaCO3-dür), maqnezitin MgCO3, dolomitin MgCO3·CaCO3, dəmir şpatı və ya sideritin FeCO3 və s.-nin tərkibinə daxildir. Üzvi birləşmələr şəklində karbon daş kömür, boz kömür, neft, təbii qaz, bitumların və s.-nin tərkibində olur.
Alınması. Karbon qrafit və almaz şəklində Yer qabığının dərin qatlarından çıxarılır. Onları süni yolla da almaq olur. Karbon kömür (koks, his və ağac kömürü) şəklində üzvi maddələrin oksigensiz şəraitdə termiki (1000°C) parçalanmasından alınır.
Fiziki xassələri. Allotrop şəkildəyişmələri. Sərbəst halda karbon bir neçə allotrop şəkildəyişmə əmələ gətirir: almaz, qrafit, karbin və füllerenlər.
1. Almaz – atom kristal qəfəsli, şəffaf, rəngsiz maddədir. Almazda karbon atomları sp3-hibridləşmə halındadır. Ona görə də almazda hər bir C atomu eyni məsafədə yerləşən 4 C atomu ilə tetraedrik olaraq birləşmişdir (a – 1). Onun kristal qəfəsində yaranan C–C σ-rabitəsi çox möhkəm rabitədir. Almazın böyük sərtliyi (bərkliyi), yüksək ərimə temperaturuna malik olması məhz C–C rabitəsinin möhkəmliyi ilə izah olunur. O, elektrik cərəyanını keçirmir. Almazdan şüşə kəsmək, dağ süxurlarını qazmaq üçün istifadə edilir.
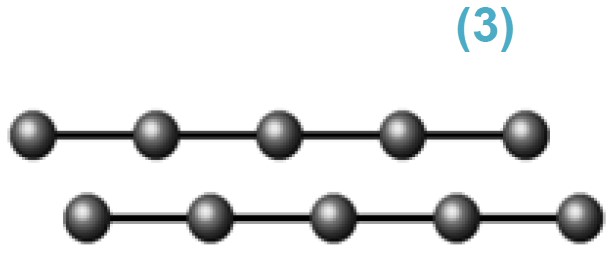
| (a) | Almaz (1), qrafit (2), karbin (3) və füllerenin C60 (4) kristal qəfəsləri. |
| (5) | – karbon əsaslı nanoboru. Onu qrafit müstəvisinin silindr şəklində bükülmüş bir forması kimi təsəvvür etmək olar. |
|
|
2. Qrafit – zəif metal parıltılı boz rəngli, yumşaq bərk maddədir. Onun kristal qəfəsində sp2-hibridləşmə halında olan C atomları düzgün altıbucaqlılardan ibarət müstəvi təbəqələrdə (laylarda) yerləşmişdir (a – 2). Təbəqələrdə hər bir C atomunun dördüncü valent elektronu metallardakı sərbəst elektronlar kimi mütəhərrik olur. Qrafitin elektrik və istilik keçirməsi, metal parıltısına malik olması məhz bununla izah edilir.
Qrafit yumşaqdır, asan qəlpələnir (kağızda iz qoyur), almaza nisbətən kimyəvi aktivdir. Lakin o, çox çətin əriyir.
O, süni yolla koksdan alınır. Qrafitdən elektrodlar, karandaşların hazırlanmasında, sürtkü materialı, nüvə reaktorlarında neytronuducu kimi istifadə edilir.
