Из двухосновных предельных карбоновых кислот в средней школе вы ознакомитесь с щавелевой и адипиновой, а из ароматических - терефталевой.
Получение. Ниже приведены схемы реакций получения щавелевой, адипиновой и терефталевой кислот:
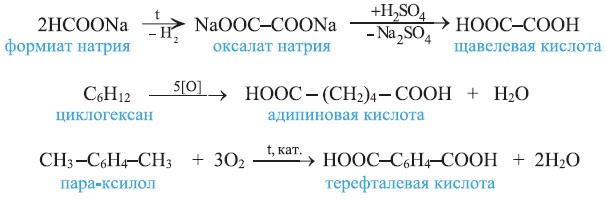
Физические свойства. Двухосновные карбоновые кислоты - кристаллические вещества белого цвета. Первые представители алкандикарбоновых кислот хорошо растворяются в воде, спирте и эфире.
Химические свойства. Двухосновные карбоновые кислоты, как и одноосновные, вступают в реакции с металлами, щелочами, спиртами. В зависимости от числа карбоксильных групп, участвующих в реакции, образуются средние или кислые соли, полные или неполные сложные эфиры, например:

При нагревании двухосновные карбоновые кислоты подвергаются декарбоксилированию (выделяют CO2). В ходе этого процесса щавелевая кислота превращается в муравьиную кислоту. При нагревании в присутствии серной кислоты щавелевая кислота разлагается с образованием трех оксидов:
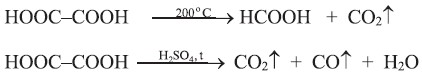
Двухосновные карбоновые кислоты сильнее соответствующих одноосновных кислот. Щавелевая кислота самая сильная из карбоновых кислот.
