При гидратации гомологов ацетилена образуются кетоны:

В промышленности ацетон получают сухой перегонкой древесины, окислением изопропилбензола и пропанола-2.
Строение. Электронное строение альдегидов на примере молекулы формальдегида приведено ниже:
Электронное строение молекулы формальдегида (a) и образование π-связи (b).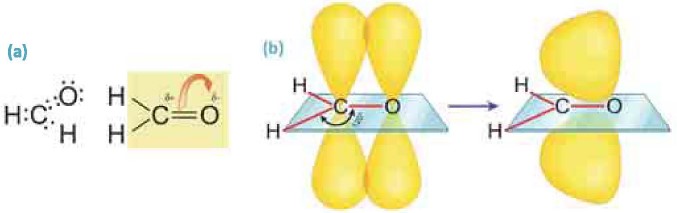
В альдегидной группе атом углерода находится в состоянии sp2-гибридизации. Три σ-связи атома углерода, направленные под углом 120° относительно друг друга, расположены в одной плоскости (a). По этой причине молекула формальдегида имеет плоское строение, р-орбиталь атома углерода, не участвующего в гибридизации путем бокового перекрывания с р-орбиталью атома кислорода, образует π-связь между углеродом и кислородом. Из-за более высокой электроотрицательности атома кислорода более подвижное π-электронное облако двойной С=O связи смещается от атома углерода в сторону атома кислорода. В результате на атоме кислорода появляется частичный отрицательный заряд  а на атоме углерода - положительный
а на атоме углерода - положительный  ∶
∶ 

Поляризация C=O связи наглядно видна на карте электронной плотности молекулы формальдегида: частичный отрицательный заряд (красная область) располагается вокруг атома кислорода, а частичный положительный (синяя область) - вокруг атома углерода.
Примечание. На карте электронной плотности двойную C=O связь указывают одним стержнем.
Поляризация >C=O связи в альдегидах проявляется в их физических и химических свойствах.
Физические свойства. Из-за отсутствия в составе альдегидов -ОН группы их молекулы не образуют между собой водородные связи. Поэтому температура кипения альдегидов ниже температуры кипения спиртов и карбоновых кислот с тем же числом атомов углерода в молекуле.