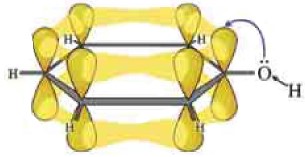
Строение молекулы. В молекуле фенола π-электронная система бензольного кольца притягивает неподеленную электронную пару атома кислорода, уменьшая электронную плотность на нем. В результате атом кислорода еще сильнее притягивает электронную плотность О-Н связи к себе.
Эти смещения электронной плотности обуславливают следующие химические свойства фенола:
1) в водном растворе отщепление водорода -ОН группы в виде протона облегчается (по сравнению с предельными спиртами) и фенол проявляет слабые кислотные свойства. По этой причине его водный раствор называют карболовой кислотой;
2) атомы водорода, связанные с атомами углерода, расположенными в положениях 2,4,6-бензольного кольца, легче замещаются на атомы брома или нитрогруппы, чем атомы водорода в самом бензоле.
• Знаете ли вы...
• Производные фенола в природе встречаются в коре тополя и ивы, в маслах тмина, мяты, гвоздики и чабреца, а также в перце.
• Производные фенола в качестве антиоксидантов добавляют к некоторым пищевым продуктам для предотвращения их быстрой порчи.
В чем состоит особенность влияния фенильной группы на -ОН группу, в отличие от алкильного радикала? Ответ подтвердите конкретными примерами.
• Взаимное влияние бензольного кольца и -ОН группы в молекуле фенола осуществляется посредством ... бензольного кольца.
• Высокая температура кипения фенола по сравнению с водой и этанолом обусловлено, главным образом, ...