Заменив в формуле CnH2n+1OH n на m+1, выразим общее число атомов в молекуле через m:
Cm+1H2(m+1)+1OH: Σ(атам) = m+1 (C) + [2(m+1)+1](H) + 1(0) + 1(H) = 3m + 6
Наличие сильнополярной O-Н связи в молекуле спиртов проявляется в их физических и химических свойствах.
Физические свойства. Спирты, содержащие до 12 атомов углерода в молекуле - жидкости, а начиная с C12H25OH и далее это - твердые вещества. Температура кипения спиртов выше температуры кипения алканов с примерно равными молекулярными массами: например, температура кипения этанола 78°С, а пропана - минус 42°С.
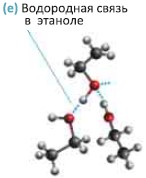
Высокая температура кипения спиртов объясняется наличием водородных связей между их молекулами (e).
С увеличением размеров молекул силы притяжения между ними возрастают; поэтому с ростом относительной молекулярной массы температура кипения спиртов увеличивается:

Метанол, этанол и пропанол-1 с водой смешиваются в любых отношениях. Это связано с образованием водородных связей между молекулами спирта и воды в их водных растворах:

С ростом молекулярной массы растворимость спиртов в воде уменьшается. Начиная с октанола (C8H17OH), спирты практически нерастворимы в воде.
Все спирты легче воды. Метанол, этанол и пропанол-1 имеют специфический алкогольный запах. Метанол очень ядовит.
О силах, влияющих на агрегатное состояние вещества.
Силы притяжения между любыми неполярными молекулами являются Вандерваальсовыми силами. Именно благодаря их наличию, алканы, состоящие из неполярных молекул - пентан, гексан и др. при комнатной температуре находятся в жидком состоянии.