| Деятельность • | Электронное строение молекул алкиламинов и аммиака. |
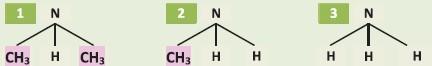
| 1 | 2 | 3 | |
| Состояние гибридизации атома азота | |||
| Число неподеленных электронных пар атома азота | |||
| Тип орбитали, содержащей неподеленную пару электронов | |||
| Вещество, которое содержит электронодонорный радикал (+) |
Получение. Предельные амины получают в основном восстановлением нитросоединений водородом:

Алкиламины получают также и действием аммиака на спирты или алкилгалогениды:

Электронное строение аминов. В молекулах аминов, как и в молекуле аммиака, атом азота находится в состоянии sp3 гибридизации и неподеленная пара электронов расположена на этой орбитали (a). Поэтому алкиламины, как и аммиак, обладают основными свойствами, т.е. амины - органические основания.
Поскольку алкильная группа, по сравнению с атомом водорода, имеет электронодонорные

свойства, то на атоме азота алкиламина электронная плотность больше, чем в случае аммиака. Поэтому алкиламины проявляют большие основные свойства, чем аммиак. С ростом числа алкильных групп в молекуле основные свойства аминов усиливаются.
Поскольку фенильная группа, по сравнению с атомом водорода, имеет электроноакцепторные свойства, то на атоме азота анилина (C6H5NH2) электронная плотность меньше, чем в случае аммиака.