Spirtlərin əksər kimyəvi xassələri onların molekulunda O-H rabitəsinin polyarlığı ilə əlaqədardır.
1. İndikatorlarla qarşılıqlı təsiri. Spirtlərin suda məhlulları indikatorların rəngini dəyişmir.
2. Metallarla qarşılıqlı təsiri. Aktiv metallar (Na, K və s.) spirtlərin -OH qrupunun hidrogenini asanlıqla əvəz edir. Reaksiya nəticəsində alman üzvi maddə alkoqolyat adlanır:
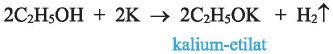
Alkoqolyatlar bərk maddələrdir. Onlar suda məhlulda hidrolizə uğrayaraq spirtə və qələviyə çevrilir:

Bu səbəbdən doymuş biratomlu spirtlər qələvi məhlulları ilə qarşılıqlı təsirdə olmur. Onların bərk qələvilərlə reaksiyası isə dönən reaksiyadır.
3. Turşularla qarşılıqlı təsiri. Spirtlər üzvi və oksigenli mineral turşularla reaksiyaya daxil olub mürəkkəb efirlər əmələ gətirir; məsələn:

Bu reaksiya efirləşmə reaksiyası adlanır. Reaksiyada su molekulunun ayrılması qatı sulfat turşusunun iştirakı ilə baş verir. Bu zaman su molekulu karbon turşusunun hidroksil qrupu ilə spirtin -OH qrupunun hidrogen atomundan əmələ gəlir
4. Spirtlərin qatı sulfat turşusunun iştirakı ilə dehidratlaşması. Spirtlər qatı sulfat turşusunun iştirakı ilə temperaturdan asılı olaraq molekuldaxili və molekullararası dehidratlaşma reaksiyasına uğrayır. Temperatur 140°C-dən yuxarı olduqda molekuldaxili dehidratlaşma baş verir və alken alınır, məsələn:
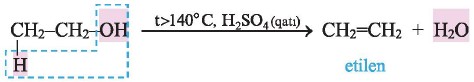
Zaytsev qaydasına görə, ikili və üçlü spirtlərin molekuldaxili dehidratlaşması zamanı hidrogen atomu, əsasən, hidrogeni az olan qonşu karbon atomundan ayrılır.