CnH2n+1OH ümumi formulunda n-i m+1 ilə əvəz edib molekulun tərkibində olan atomların ümumi sayını m ilə ifadə edək:
Cm+1H2(m+1)+1OH: Σ(atom) = m+1 (C) + [2(m+1)+1](H) + 1(0) + 1(H) = 3m + 6
Spirt molekulunda güclü polyar O-H rabitəsinin olması spirtlərin fiziki və kimyəvi xassələrində özünü göstərir.
Fiziki xassələri. Molekullarında 12-yə qədər karbon atomu olan spirtlər maye, C12H25OH və sonrakı spirtlər isə bərk maddələrdir. Spirtlərin qaynama temperaturları təxminən eyni molekul kütləli alkanların qaynama temperaturlarından yüksəkdir: məsələn, etanolun (Mr(C2H5OH) = 46) qaynama temperaturu 78°C, propanınkı (Mr(C3H8) = 44) isə mənfi 42°C-dir.
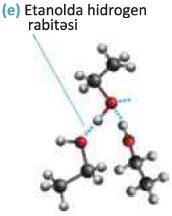
Spirtlərin yüksək qaynama temperaturuna malik olması spirt molekullarının öz aralarında hidrogen rabitəsi əmələ gətirməsi ilə izah edilir (e).
Böyük molekullar arasında cazibə qüvvələri artdığından spirtlərin nisbi molekul kütlələri artdıqca onların qaynama temperaturları da artır:

Metanol, etanol və propanol-1 su ilə istənilən nisbətdə qarışır. Bu hadisə məhlulda spirt və su molekullan arasında hidrogen rabitəsinin yaranması ilə əlaqədardır:

Molekul kütləsi artdıqca spirtlərin suda həll olması azalır. Oktanoldan (C8H17OH) başlayaraq spirtlər suda praktik həll olmur.
Bütün spirtlər sudan yüngüldür. Metanol, etanol və propanol-1 xüsusi alkoqol iyinə malikdir. Metil spirti çox zəhərlidir.
Maddənin aqreqat halına təsir edən qüvvələr haqqında.
İstənilən qeyri-polyar molekullar arasında təsir edən cazibə qüvvələri - Van der Vaals qüvvələridir. Məhz bu qüvvələrin təsiri nəticəsində qeyri-polyar molekullu alkanlar - pentan, heksan və s. otaq temperaturunda maye haldadır.