2. При растворении соли CuCl2 dв воде происходит электролитическая диссоциация. В растворе образовались свободные носители зарядов: положительные ионы меди (Cu2+) и отрицательные ионы хлора (Cl–). При замыкании цепи положительные ионы, двигаясь к катоду, и отрицательные ионы, двигаясь к аноду, осуществили электрический ток через раствор. Делая из этого выводы, можно дать следующее определение электролитам:
• Электролиты - это вещества, расплавы или растворы, проводящие электрический ток за счет ионов, образовавшихся вследствие диссоциации.
• Электролиты - это вещества, расплавы или растворы, проводящие электрический ток за счет ионов, образовавшихся вследствие диссоциации.
• Так как электрический ток в электролитах представляет собой упорядоченное движение ионов, то такую проводимость называют ионной.
3. При замыкании цепи дошедшие до анода ионы хлора Cl–, отдав свой лишний электрон электроду, нейтрализуются реакцией окисления и выделяются на поверхности анода в виде пузырьков:
2Cl— — 2e— → Cl2.
Дошедшие до катода ионы меди Cu2+, забирая у этого электрода по два электрона, превращаются в нейтральные атомы меди и, откладываясь на аноде, образуют на нем слой меди: Cu2+ + 2e— → Cu0. Происходит процесс электролиза. Значит, прохождение тока через раствор электролита сопровождается выделением вещества на электродах.
Сила тока, проходящего через электролит, при постоянном значении сопротивления линейно зависит от напряжения - закон Ома для электролитов выполняется (a). Однако график не пересекает начало координат, он несколько смещен вправо. Это объясняется тем, что некоторое значение напряжения идет на поляризацию опущенных в раствор электролита электродов.
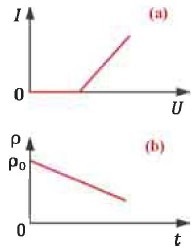
Поляризация электродов - отклонение заряда электрода от его равновесного значения в процессе электролиза. В результате поляризации от своего равновесного значения отклоняются и значения потенциалов электродов.
С ростом температуры сопротивление (удельное сопротивление) электролита линейно уменьшается. Это происходит потому, что с ростом температуры интенсивность теплового движения частиц в растворе электролита увеличивается и соответственно растет степень диссоциации
(b):
ρ = ρ0(1 +αt).
Здесь α — температурный коэффициент сопротивления, он обладает отрицательным значением, ρ0 — значение удельного сопротивления электролита при 0°С.
Закон электролиза. Этот закон в 1836 году был выдвинут английским ученым М.Фарадеем. В нем установлена закономерная зависимость между величинами, характеризующими явление электролиза. Эту зависимость можем определить и мы. Для этого обозначим массу иона moi, количество дошедших до катода за время Δt ионов Ni:
m = moi • Ni. (1)
Масса иона определяется на основе значения молярной массы химического элемента:
moi = M
NA. (2)
Здесь NA — число Авогадро, M — молярная масса химического элемента. Количество дошедших до катода ионов за время Δt равно отношению заряда Δq, прошедшего за это время через раствор к заряду иона (qoi):