ЗАКОН ЭЛЕКТРОЛИЗА
|
• ВСПОМНИТЕ ПРОЙДЕННОЕ •
Физика - 9 |
|
- Процесс распада в жидкости нейтральных молекул на положительные и отрицательные ионы называется электролитической диссоциацией.
- Электрический ток в электролитах представляет собой упорядоченное движение положительных и отрицательных ионов.
- Процесс выделения вещества на электродах при прохождении электрического тока через электролит называется электролизом.
- Масса вещества, выделенного на электродах при электролизе, прямо пропорциональна заряду, прошедшему через электролит. Этот закон электролиза, установленный английским ученым М. Фарадеем, математически выражается следующим образом:
m = k • q или m = kIt.
- Электрохимический эквивалент вещества численно равен массе вещества, выделившегося на электроде при прохождении через электролит заряда 1 Кл. Разные вещества обладают различным значением электрохимического эквивалента.
| ■ |
Неотъемлемой частью огромного количества современных устройств, от мобильных телефонов до автомобилей, являются электрохимические элементы и аккумуляторы.
В гигантских электролитических ваннах, испаряющих ядовитые пары, из расплавленных при высоких температурах бокситов методом электролиза получают алюминий, используемый в дальнейшем для изготовления от обычной банки для колы до авиационной промышленности. Вокруг нас много предметов, покрытие которых осуществлено методом электролиза (ювелирные изделия, хромированные ручки дверей и окон и др.). Не случайно это явление изучается в отдельном разделе науки - электрохимии. |
| ИССЛЕДОВАНИЕ | 1 |
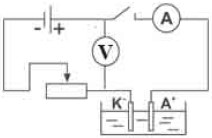
Оборудование: источник постоянного тока (выпрямитель ВС-24), электролитическая ванна, дистиллированная вода, соль
CuCl2, амперметр, вольтметр, ключ, реостат, соединительные провода.
Ход работы:
1. Соберите электрическую цепь по приведенной схеме.
2. Налейте в электролитическую ванну дистиллированной воды и замкните цепь, наблюдая за показаниями электроизмерительных приборов.
3. Разомкните цепь, добавьте в воду немного соли CuCl2. Замкнув снова цепь, следите за показаниями приборов.
Обсуждение результата:
• Каков результат вашего опыта?
• Объясните процесс явления электролиза при добавлении в воду соли CuCl2.
• Какие частицы электроносителей обеспечили электропроводность в солевом растворе?
Явление электролиза. Опыт приводит к следующим выводам:
1. Жидкости, как и газы, могут быть как диэлектриками, так и проводниками.