Все состояния атома с n > 1 являются возбужденными состояниями. Атом не может существовать продолжительное время в возбужденном состоянии и, излучив энергию, возвращается в основное состояние.
Таким образом, согласно формуле (3), энергия атома водорода в первом квантовом состоянии
E1 = -E0, во втором E2 = - E0
22, в третьем
E3 = - E0
32 т.д. Это
значит, что при переходе атома водорода из состояния с минимальной энергией во второе энергетическое состояние его энергия увеличивается в 4 раза, при переходе в третье энергетическое состояние - в 9 раз и т.д.
Энергетические уровни атома изображаются горизонтальными линиями. Переход атома из одного стационарного состояния в другое изображается вертикальными стрелками: направленная вниз стрелка соответствует излучению одного кванта энергии, направленная вверх стрелка соответствует поглощению одного кванта энергии (e).

Из диаграммы энергетических уровней атома видно, что в квантовом состоянии n = ∞ его энергия E∞ = 0. Это означает, что электрон, прервав связь с ядром, в свободном состоянии находится в покое. Поэтому энергетические уровни электронов, связанных с ядром, должны быть меньше нуля, соответствуя отрицательным значениям. Так как электрон притягивается ядром, то для отрыва его от ядра необходимо совершить положительную работу.
Согласно III постулату Бора возможные частоты излучения атома водорода определяются формулой:
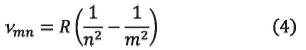
Здесь R ≈ 3,3 ⋅ 1015с-1 — постоянная Ридберга. Экспериментально установлено, что при переходе электрона в атоме водорода с верхних энергетических уровней на второй уровень происходит излучение фотона видимого света.