Квантовые постулаты Бора. В 1913 году датский ученый Нильс Бор (1885- 1962) опубликовал свои работы по квантовой теории атома, основанные на гипотезе Планка о световых квантах. В этой публикации он с помощью 3-х постулатов устранил затруднения планетарной модели атома на основе квантовых представлений.
В первом постулате Бор обосновывает существование состояний, в которых ускоренно движущийся электрон не излучает электромагнитные волны.
• I постулат - атом может существовать не в состояниях, подчиняющихся законам классической физики, а только в особых квантовых (или в стационарных) состояниях. Каждому квантовому состоянию соответствует определенная Еn энергия. В стационарном состоянии атом не излучает электромагнитные волны (b).
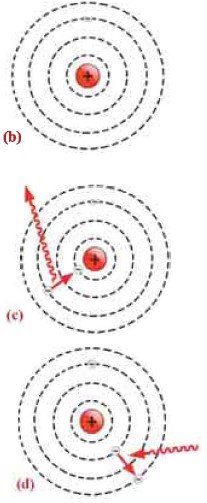
Второй постулат Бора объясняет процессы поглощения и излучения света атомом.
• II постулат - при переходе из одного стационарного состояния в другое атом поглощает или излучает один квант света, энергия которого равна hvmn. Энергия поглощенного ши излученного кванта равна разности энергий этих стационарных состояний:
hvmn = Em - En. (1)
Отсюда для частоты излучения получаем:
Vmn = (Em - En)
h = Em
h - En
h.
(2)
При переходе атома из стационарного состояния с большей энергией в стационарное состояние с меньшей энергией происходит излучение: Em < En.
В этом случае электрон, излучая один квант света, переходит с удаленной от ядра орбиты на орбиту, близкую к ядру (c).
Поглотив один квант света, атом переходит из стационарного состоянш с меньшей энергией в стационарное состояние с большей энергией:
Em > En.
В этом случае электрон переходит с орбиты, близкой к ядру, на орбиту, удаленную от ядра (d).
Энергетические уровни атома. Для стационарных состояний атома водорода Бор вывел следующую формулу:
En = - E0
n2. (3)
Здесь E0 = 13,6 эВ - энергия ионизации атома водорода в состоянии с минимальной энергией, n — главное квантовое число. Стационарное состояние с главным квантовым числом n = 1 является основным состоянием атома, и в этом состоянии он не излучает энергию.